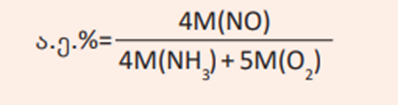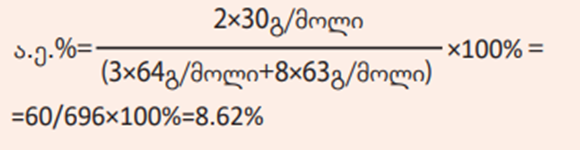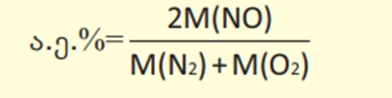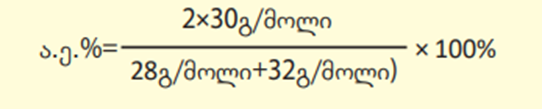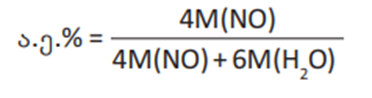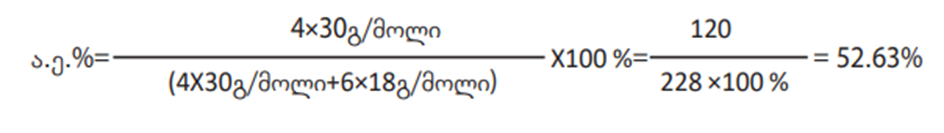„განათლება მდგრადი განვითარებისთვის“ (ESD) ეს არის UNESCO-ს განათლების დეპარტამენტის პასუხი დედამიწის წინაშე მდგარ გადაუდებელ გამოწვევებზე. ევროკავშირის მიერ შემუშავებული საინიციატივო წინადადებები „მწვანე მიზნები“, 2050 წლისთვის ევროპის მდგრადობასა და უსაფრთხო კლიმატის შენარჩუნებას გულისხმობს. მნიშვნელოვანია სკოლას ჰქონდეს გარკვეული ხედვა მდგრადი განვითარების მიზნების დანერგვასთან დაკავშირებით. თუმცა ეს არ უნდა იყოს ცალკე საგანი, რომელიც სასკოლო გეგმის გადატვირთვას გამოიწვევს. უდიდესი როლი მასწავლებელს ენიჭება, რომელსაც საკუთარ გაკვეთილზე შეუძლია საკითხი განიხილოს გამჭოლი კომპეტენციის ჭრილში. გთავაზობთ ქიმიის ერთი გაკვეთილს მეცხრე კლასის მოსწავლეებისთვის.
სამიზნე ცნება: აღმოჩენა, თეორია, კანონი, მდგრადი განვითარება, ტექნოლოგია;
ინდიკატორი: ქიმ.საბ.12. საბუნებისმეტყველო მეცნიერებების და ტექნოლოგიების მიღწევების შეფასება მდგრადი განვითარების პრინციპების თვალსაზრისით;
გაკვეთილის ბოლოს მოსწავლე შეძლებს:
- იმსჯელოს მდგრადი განვითარების მიზნების მნიშვნელობაზე;
- ექსპერიმენტის დაგეგმვის დროს დაიცვას მწვანე ქიმიის 12 პრინციპი;
- ამოხსნას ამოცანა ატომეკონომიის გათვალისწინებით.
ლექსიკონი:
- მდგრადი განვითარება – პირობების შექმნა გრძელვადიანი ეკონომიკური განვითარებისათვის გარემოს დაცვის საკითხების მაქსიმალური გათვალისწინებით.
- მწვანე ქიმია – ქიმიური პროდუქციის წარმოება, რომლის დროსაც მინიმუმამდეა შემცირებული გარემოსა და ადამიანის ჯანმრთელობაზე მავნე ქიმიური ნაერთების ზემოქმედება.
სამოტივაციო ტექსტი:
ცივგომბორის კალთები საოცრად ფერადია შემოდგომაზე.
ამ სილამაზის საფუძველი რომ ქიმიური ნაერთებია, ალბათ შენთვის უკვე ცნობილია. ქიმიის ერთ მიმართულებასაც ჰქონია თავისი ფერი და მას მწვანე ქიმიას უწოდებენ. მსოფლიოში შექმნილმა გლობალურმა ეკოლოგიურმა პრობლემებმა, მდგრადი განვითარების მიზნების ფარგლებში, მეცნიერებს დაანახა მწვანე ქიმიის განვითარების აუცილებლობა.
მაინც რა არის მწვანე ქიმია?
მწვანე ქიმია ქიმიის მიმართულებაა, რომელიც:
- ხელს უშლის გარემოს დაბინძურებას მოლეკულურ დონეზე;
- გავლენას ახდენს ქიმიის ყველა მიმართულებაზე;
- გარემოსდაცვითი პრობლემების მოგვარებაში იყენებს თანამედროვე მეთოდებს;
- ხელს უშლის ნიადაგის, წყლისა და ჰაერის დამაბინძურებლების წარმოქმნას;
- ამცირებს ქიმიური პროდუქტებისა და პროცესების გავლენას ადამიანის ჯანმრთელობაზე.
რა კავშირია მდგრად განვითარებასა და მწვანე ქიმიას შორის?
2011 წლის ოქტომბერში ადამიანის პოპულაციამ 7 მილიარდი შეადგინა. პლანეტაზე ბევრი ადამიანი ნიშნავს გაზრდილ მოთხოვნილებას რესურსებზე, მათ შორის საკვებსა და წყალზე. პოპულაციის ჯანმრთელობისთვის აუცილებელია ხელმისაწვდომი იყოს საკვები, წყალი, ტერიტორია. რა მოხდება, როცა მოსახლეობისთვის რესურსი იქნება აღარ საკმარისი? ამ საკითხებზე მსჯელობის დროს ჩამოყალიბდა მდგრადი განვითარების მიზნები, რომელიც მოიცავს 17 მიზანსა და 169 ინდიკატორს, რომელზეც შეთანხმებულია გაეროს წევრი ყველა ქვეყანა უკეთესი და უფრო მდგრადი მომავლის მისაღწევად. მწვანე ქიმიის მიზანი ისეთი ქიმიური პროცესების წარმართვა და პროდუქტების შექმნაა, რომელიც არ დააბინძურებს გარემოს და ადამიანის ჯანმრთელობას; საფრთხეს არ შეუქმნის ცხოველთა და მცენარეთა სახეობების არსებობას ეკოსისტემაში. მეცნიერების შეთანხმებით ჩამოყალიბდა მწვანე ქიმიის 12 პრინციპი:
- იფიქრე ნარჩენების პრევენციაზე – სასურველია რეაქციები წარიმართოს თანაური პროდუქტების რაოდენობის შემცირების მიმართულებით, რათა თავიდან ავიცილოთ მათი უტილიზაციისთვის საჭირო ხარჯი.
- რეაქციები დაგეგმე მაქსიმალური ატომეკონომიით/ატომეფექტურობით – ქიმიური რეაქციები უნდა წარიმართოს ისე, რომ რეაგენტებში შემავალი ატომები მაქსიმალურად მოხვდნენ სასურველ პროდუქტში.
- გამოიყენე არატოქსიკური რეაქტივები – ექსპერიმენტებისთვის უნდა გამოიყენო ადამიანის ჯანმრთელობისთვის და გარემოსთვის ნაკლებად საზიანო ქიმიური ნაერთები.
- მიიღე არატოქსიკური პროდუქტები – ექსპერიმენტებისთვის უნდა გამოიყენო ისეთი ნაერთები, რომელთა ურთიერთქმედებით მიიღება ადამიანის ჯანმრთელობისა და გარემოსთვის ნაკლებად საზიანო ქიმიური ნაერთები.
- გამოიყენე არატოქსიკური გამხსნელები – რეაქცია უმჯობესია ჩატარდეს გამხსნელის გარეშე. თუ გამხსნელი აუცილებელია, უმჯობესია გამოყენებული იყოს არატოქსიკური გამხსნელი.
- შეამცირე ენერგიის ხარჯი – დაგეგმე ისეთი რეაქციები, რომლებიც მიმდინარეობს ოთახის ტემპერატურაზე ან საჭიროებს ენერგიის მცირე რაოდენობას.
- ისარგებლე აღდგენადი რესურსებით – რეაქციებისთვის გამოიყენე მცენარეული პროდუქტები ან სხვა რეაქციების დროს მიღებული ნარჩენები.
- შეამცირე შუალედური პროდუქტები – მრავალსაფეხურიან პროცესებში ბევრი შუალედური პროდუქტი წარმოიქმნება. დაგეგმე ისეთი რეაქციები, სადაც ნაკლები ეტაპის გავლა იქნება საჭირო.
- გამოიყენე კატალიზატორი – კატალიზატორი ამცირებს რეაქციისთვის საჭირო ტემპერატურას, ამით დაიზოგება ენერგია.
- მოახდინე ნარჩენების უტილიზაცია – რეაქციების დაგეგმვის დროს გაითვალისწინე, რომ მიღებული პროდუქტები იყოს ბიოდეგრადირებადი და არ აზიანებდეს გარემოს.
- თავიდან აიცილე გარემოს დაბინძურება – გაითვალისწინე რომ გარემოში გამოყოფილი ნაერთები ნაკლებად აზიანებდნენ გარემოს.
- დაიცავი უსაფრთხოება – დაგეგმე ისეთი ექსპერიმენტები, რომლებიც არ არის საფრთხის შემცველი; ექსპერიმენტები ჩაატარე უსაფრთხოების წესების სრული დაცვით.
რეაქციის შეფასება ატომეკონომიის თვალსაზრისით
თანამედროვე მსოფლიო წარმოუდგენელია ქიმიური წარმოების გარეშე. მწარმოებელი ვალდებულია დაიცვას მწვანე ქიმიის პრინციპები, მათ შორის ატომეფექტურობის პრინციპი. თუ ნაერთის მიღება შესაძლებელია რამდენიმე ქიმიური ტოლობის შესაბამისად, უნდა შეირჩეს ის პროცესი, რომელიც ატომეკონომიურია, დანარჩენებთან შედარებით.
როგორ დავადგინოთ ატომეფექტურობა?
I ხერხი
! რეაქციის ტოლობა უნდა იყოს გათანაბრებული.
! ფორმულაში გაითვალისწინე რეაქციის ტოლობაში მოცემული კოეფიციენტები.
ამოცანა: აზოტის ოქსიდის მისაღებად სამი რეაქციიდან შეარჩიე ყველაზე ატომეკონომიური პროცესი.
4NH3 + 5O2 4NO + 6H2O (I)
3Cu + 8HNO3 3Cu(NO3)2 + 2 NO + 4H2O (II)
N2 + O2 2 NO (III)
განვიხილოთ I ტოლობა
რეაქციის შედეგად მიიღება ორი პროდუქტი. NO-ს წინ კოეფიციენტია 4, ამიაკის წინ – 4 და ჟანგბადის წინ – 5. ამიტომ ფორმულა ასე გამოისახება:
ა.ე.% = 4 M (NO) / (4M(NH3) + 5M(O2 ))
M (NO) = 14გ/მოლი + 16 გ/მოლი = 30გ/მოლი
M(NH3) = 17 გ/მოლი
M(O2) = 32 გ/მოლი
ა.ე.% = 4 X30 გ/მოლი / (4X17გ/მოლი + 5X 32 გ/მოლი) X 100 % = 120/228 X100 % =52.63%
განვიხილოთ II ტოლობა
რეაქციის შედეგად მიიღება ორი პროდუქტი
ა.ე.% = 4 M (NO) / (4M(NH3) + 5M(O2))
M (NO) = 14გ/მოლი + 16 გ/მოლი = 30გ/მოლი
M(Cu) = 64 გ/მოლი
M(HNO3) = 63 გ/მოლი
განვიხილოთ III ტოლობა
რეაქციის შედეგად მიიღება მხოლოდ ერთი პროდუქტი. ივარაუდე რას უნდა უდრიდეს რეაქციის ატომეფექტუროობა?
M (NO) = 14გ/მოლი + 16 გ/მოლი = 30გ/მოლი
M(N2) = 28 გ/მოლი
M(O2) = 32 გ/მოლი
შეაფასე შედეგი: რომელი ტოლობა გამოსახავს ყველაზე ატომეკონომიურ რეაქციას? რატომ?
დასკვნა: ყველაზე ეფექტურია მესამე ტოლობა, რადგან მხოლოდ ერთი პროდუქტი მიიღება. ამიტომ თუ არსებობს სასურველი პროდუქტის შეერთების რეაქციის გზით მიღების საშუალება, მის გამოყენებას მიენიჭება უპირატესობა.
თუმცა რეაქციის შერჩევის დროს ატომეკონომიურობასთან ერთად მწვანე ქიმიის სხვა პრინციპების გათვალისწინებაა აუცილებელი და გადაწყვეტილება კომპლექსურად უნდა იქნეს მიღებული.
II ხერხი
ატომეკონომია % = სასურველი პროდუქტის მოლური მასა / პროდუქტების მოლური მასების ჯამი X 100 %
! რეაქციის ტოლობა უნდა იყოს გათანაბრებული.
! ფორმულაში გაითვალისწინე რეაქციის ტოლობაში მოცემული კოეფიციენტები.
განვიხილოთ ისევ ამიაკის წვის ტოლობა 4NH3 + 5O2 4 NO + 6H2O.
რეაქციის შედეგად მიიღება ორი პროდუქტი. NO-ს კოეფიციენტია 4, წყლის – 6. ამიტომ ფორმულა ასე გამოისახება:
M (NO) = 14გ/მოლი + 16 გ/მოლი = 30გ/მოლი
M(H2O) = 18 გ/მოლი
დავალება:
- მოცემულ ქიმიურ ტოლობებში შეარჩიე კოეფიციენტები და დაადგინე ატომეკონომია, თუ სასურველი პროდუქტია NaOH
ა) Na + H2O NaOH + H2
ბ) Na2O + H2O NaOH
დ) Na2SO4 + Ba(OH)2 NaOH + BaSO4
- გაიხსენე შეერთების, დაშლის, ჩანაცვლებისა და მიმოცვლის რეაქციები და იმსჯელე, რომელი რეაქციაა ყველაზე მეტად ატომეკონომიური?
- გოგირდმჟავა ქიმიური წარმოების ერთ-ერთი ძირითადი პროდუქტია. მის მისაღებად რამდენიმე ეტაპის გავლაა საჭირო. პირველ საფეხურს გოგირდის დიოქსიდის მიღება წარმოადგენს. შეადგინე გოგირდის დიოქსიდის მიღების რეაქციის ტოლობა სამი სხვადასხვა ხერხით და შეაფასე ატომეკონომიურობა და დაუსაბუთე მწარმოებელს, რომელი რეაქცია გამოიყენოს. დაასაბუთე შენი არჩევანი.
- ბოლო წლებში ავარიების შედეგად გარდაცვლილთა რაოდენობის შემცირება შესაძლებელი გახდა ,,აირის ჩანთის“ გამოყენებით. მოიძიე ინფორმაცია და სიმულაციის დახმარებით https://bit.ly/3oHlxxt
მოამზადე მისი მოქმედების ამსახველი პოსტერი. პოსტერში წარმოადგინე:
- რა ქიმიური პროცესი მიმდინარეობს აირის ჩანთის გაბერვისას?
- რეაქციათა რომელ ტიპს მიეკუთვნება ის?
- რა მასალისგან არის დამზადებული აირის ჩანთა და რატომ? მწვანე ქიმიის რომელი პრინციპის დაცვა ხდება ,,Air Bag”-ისთვის მასალის შერჩევის დროს? გაითვალისწინე, რომ მსოფლიოში ექსპლუატაციაში მყოფი ავტომობილების უმრავლესობას საერთოდ არ ეხსნება აირის ჩანთა.
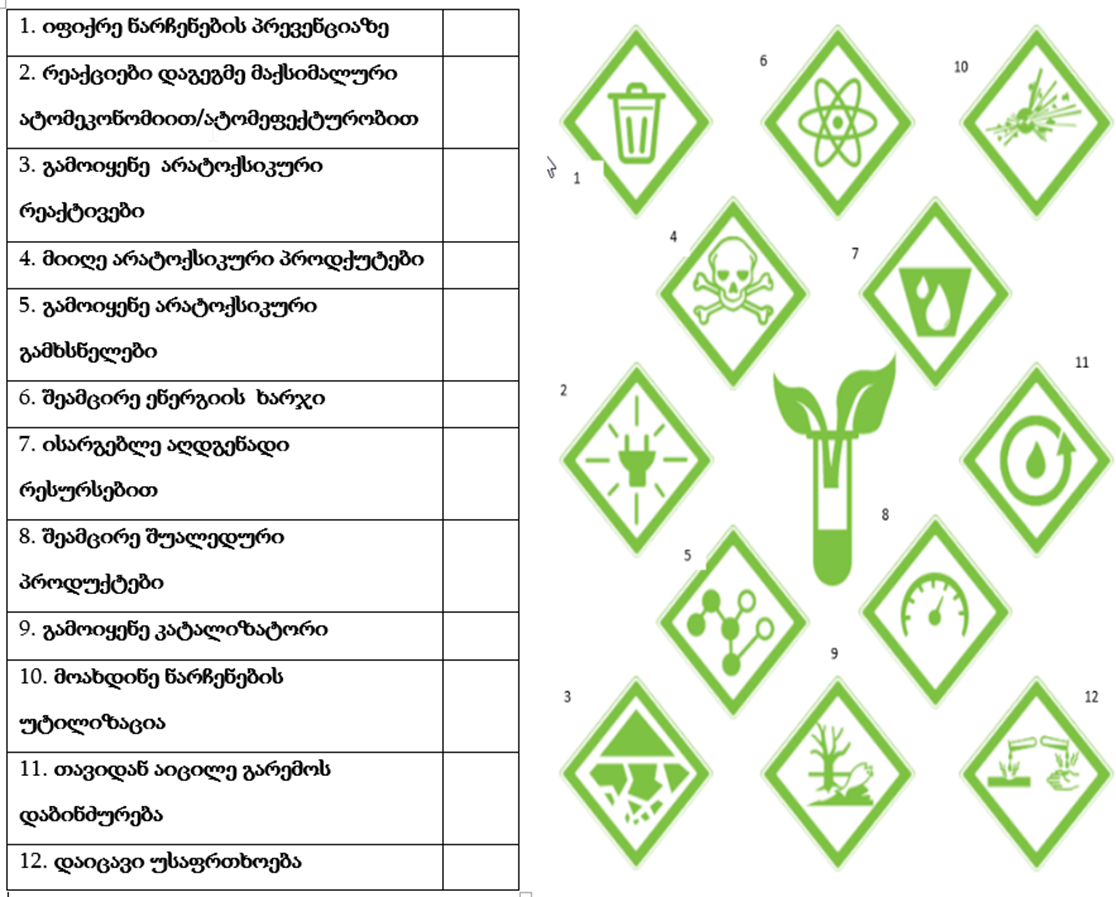
- ჩამოთვლილი 12 პრინციპი შეუსაბამე პიქტოგრამას და ცხრილის შესაბამის უჯრაში ჩაწერე პიქტოგრამის ნომერი.
გამოყენებული ლიტერატურა:
- https://chemistry.ge/publication/chemnews/view.php?id=226
- https://greenalt.org/app/uploads/2013/12/mwvane_politika_da_garemos_dacva.pdf
- მესამე თაობის ესგ, ქიმიის სტანდარტი.